《山東省濟寧市第十三中學(xué)2020屆九年級化學(xué)全冊 專題一 物質(zhì)構(gòu)成的奧秘練習(xí)(無答案) 魯教版五四制》由會員分享�����,可在線閱讀����,更多相關(guān)《山東省濟寧市第十三中學(xué)2020屆九年級化學(xué)全冊 專題一 物質(zhì)構(gòu)成的奧秘練習(xí)(無答案) 魯教版五四制(2頁珍藏版)》請在裝配圖網(wǎng)上搜索�。
1、專題一 物質(zhì)構(gòu)成的奧秘
知識整合
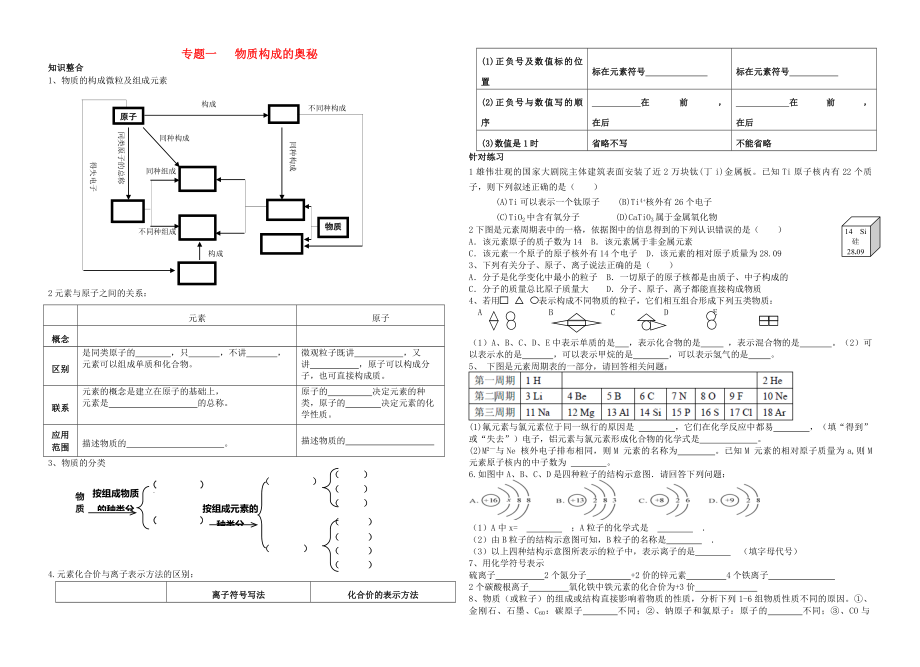
1�����、物質(zhì)的構(gòu)成微粒及組成元素
不同種組成
同種構(gòu)成
不同種構(gòu)成
同種組成
同類原子的總稱
同種構(gòu)成
構(gòu)成
原子
物質(zhì)
得失電子
構(gòu)成
2元素與原子之間的關(guān)系:
元素
原子
概念
區(qū)別
是同類原子的 �����,只 ��,不講 �����,元素可以組成單質(zhì)和化合物�。
微觀粒子既講 ,又講 ,原子可以構(gòu)成分子�,也可直接構(gòu)成質(zhì)。
聯(lián)系
元素的概念是建立在原子的基礎(chǔ)上����,
元素是
2、 的總稱�。
原子的 決定元素的種類,原子的 決定元素的化學(xué)性質(zhì)����。
應(yīng)用
范圍
描述物質(zhì)的 。
描述物質(zhì)的
3����、物質(zhì)的分類
物質(zhì)
( ) )
( )
按組成元素的種類分
( )
( )
( )
按組成物質(zhì)的種類分
( )
( )
( )
( )
( )
( )
4.
3、元素化合價與離子表示方法的區(qū)別:
離子符號寫法
化合價的表示方法
(1)正負(fù)號及數(shù)值標(biāo)的位置
標(biāo)在元素符號
標(biāo)在元素符號
(2)正負(fù)號與數(shù)值寫的順序
在前�����, 在后
在前��, 在后
(3)數(shù)值是1時
省略不寫
不能省略
針對練習(xí)
1雄偉壯觀的國家大劇院主體建筑表面安裝了近2萬塊鈦(丁i)金屬板��。已知Ti原子核內(nèi)有22個質(zhì)子�,則下列敘述正確的是( )
(A)Ti可以表示一個鈦原子 (B)Ti4+核外有26個
4��、電子
14 Si
硅
28.09
(C)TiO2中含有氧分子 (D)CaTiO3屬于金屬氧化物
2下圖是元素周期表中的一格�����,依據(jù)圖中的信息得到的下列認(rèn)識錯誤的是( )
A.該元素原子的質(zhì)子數(shù)為14 B.該元素屬于非金屬元素
C.該元素一個原子的原子核外有14個電子 D.該元素的相對原子質(zhì)量為28.09
3�、下列有關(guān)分子�、原子��、離子說法正確的是( )
A.分子是化學(xué)變化中最小的粒子 B.一切原子的原子核都是由質(zhì)子���、中子構(gòu)成的
C.分子的質(zhì)量總比原子質(zhì)量大 D.分子�����、原子���、離子都能直接構(gòu)成物質(zhì)
4、若用表示構(gòu)成不同物質(zhì)的粒子
5���、���,它們相互組合形成下列五類物質(zhì):
A B C D E
(1)A、B、C�、D、E中表示單質(zhì)的是 ��,表示化合物的是 �,表示混合物的是 。(2)可以表示水的是 �,可以表示甲烷的是 ,可以表示氫氣的是 �。
5、 下圖是元素周期表的一部分���,請回答相關(guān)問題:
(1)氟元素與氯元素位于同一縱行的原因是 ����,它們在化學(xué)反應(yīng)中都易 ���,(填“得到”或“失去”)電子�,鋁元素與氯元素形成化合物的化學(xué)式是
6�、 。
(2)M2—與Ne 核外電子排布相同�����,則M 元素的名稱為 。已知M 元素的相對原子質(zhì)量為a,則M 元素原子核內(nèi)的中子數(shù)為 �����。
6.如圖中A���、B�����、C�����、D是四種粒子的結(jié)構(gòu)示意圖.請回答下列問題:
(1)A中x= �����;A粒子的化學(xué)式是 ?�。?
(2)由B粒子的結(jié)構(gòu)示意圖可知�,B粒子的名稱是 .
(3)以上四種結(jié)構(gòu)示意圖所表示的粒子中�,表示離子的是 ?����。ㄌ钭帜复枺?
7�、用化學(xué)符號表示
硫離子 2個氮分子 +2價的鋅元素 4個鐵離子
2個碳酸根離子 氧化鐵中鐵元素的化合價為+3價
8��、物質(zhì)(或粒子)的組成或結(jié)構(gòu)直接影響著物質(zhì)的性質(zhì)�����,分析下列1-6組物質(zhì)性質(zhì)不同的原因�。①、金剛石��、石墨��、C60:碳原子 不同�����;②�、鈉原子和氯原子:原子的 不同;③�����、CO與CO2 :分子的 不同;④���、生鐵和鋼: 不同�;
⑤�����、酸溶液和堿溶液所含的 不同��;⑥���、氧元素和碳元素: 不同�����;
 山東省濟寧市第十三中學(xué)2020屆九年級化學(xué)全冊 專題一 物質(zhì)構(gòu)成的奧秘練習(xí)(無答案) 魯教版五四制
山東省濟寧市第十三中學(xué)2020屆九年級化學(xué)全冊 專題一 物質(zhì)構(gòu)成的奧秘練習(xí)(無答案) 魯教版五四制