《重慶市璧山縣青杠初級(jí)中學(xué)校九年級(jí)化學(xué)上冊(cè) 第三單元 課題1 分子和原子復(fù)習(xí)學(xué)案(無(wú)答案)(新版)新人教版》由會(huì)員分享��,可在線閱讀����,更多相關(guān)《重慶市璧山縣青杠初級(jí)中學(xué)校九年級(jí)化學(xué)上冊(cè) 第三單元 課題1 分子和原子復(fù)習(xí)學(xué)案(無(wú)答案)(新版)新人教版(3頁(yè)珍藏版)》請(qǐng)?jiān)谘b配圖網(wǎng)上搜索�。
1、分子和原子
一����、教學(xué)要求
學(xué)習(xí)目標(biāo)
1、知識(shí)與技能(1) 知道原子的構(gòu)成��。
(2) 知道相對(duì)原子質(zhì)量����、元素、離子的概念����,
(3) 能區(qū)分分子�����、原子�、離子的區(qū)別���。
(4)知道物質(zhì)由于微小的粒子構(gòu)成的�。能用粒子的性質(zhì)解釋日常生活中的一 些現(xiàn)象�。
教學(xué)重點(diǎn)、難點(diǎn):(1)原子的構(gòu)成�。
(2)知道物質(zhì)由于微小的粒子構(gòu)成的。能用粒子的性質(zhì)解釋日常生活 中的一些現(xiàn)象�����。
2��、 (3)微觀知識(shí)的應(yīng)用����。
(4)運(yùn)用原子��、分子、元素描述物質(zhì)的組成或粒子的構(gòu)成
學(xué)法指導(dǎo):討論總結(jié)――補(bǔ)充講解――練習(xí)提高
二����、自主學(xué)習(xí)
(一)、物質(zhì)的微粒性
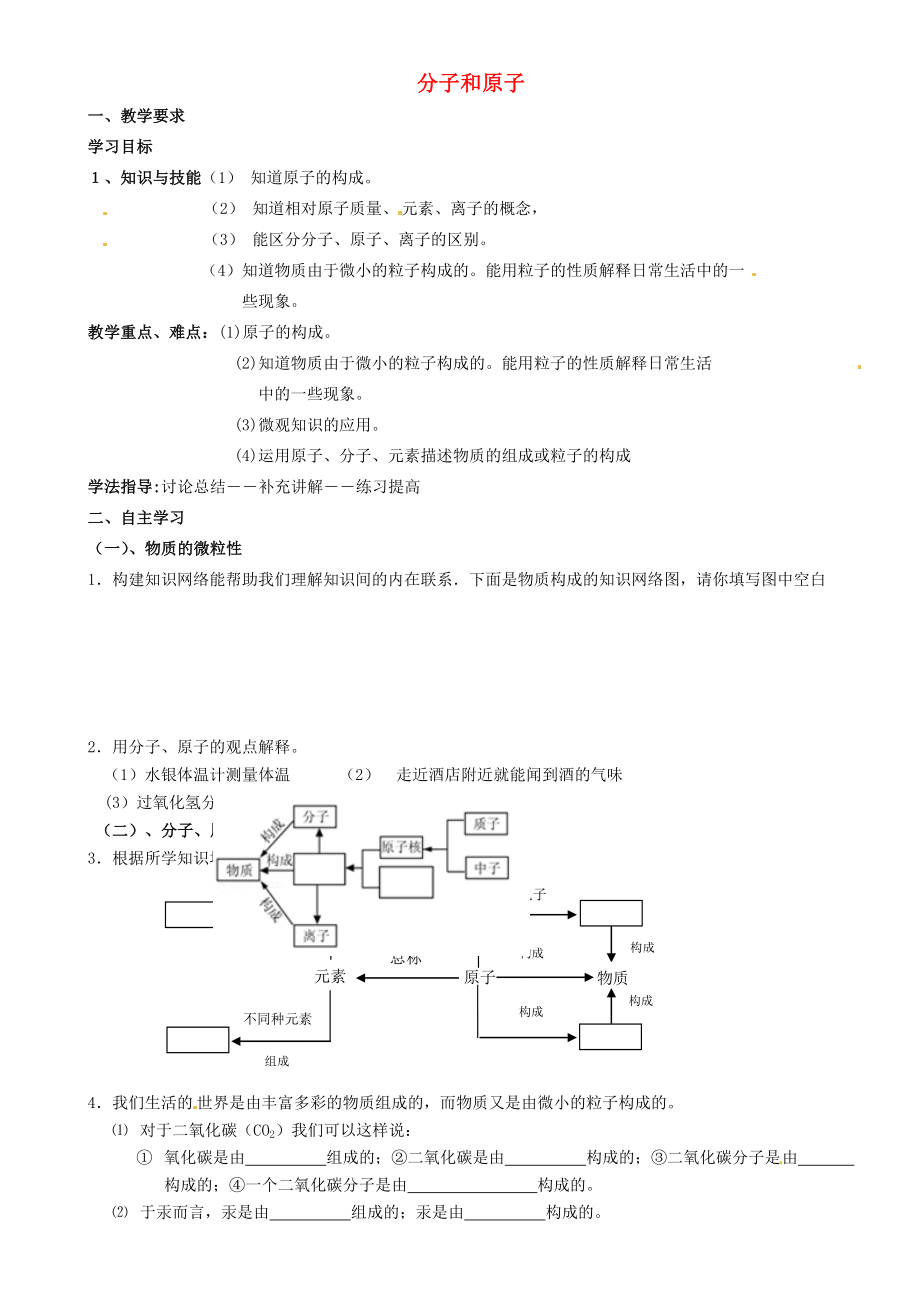
1.構(gòu)建知識(shí)網(wǎng)絡(luò)能幫助我們理解知識(shí)間的內(nèi)在聯(lián)系.下面是物質(zhì)構(gòu)成的知識(shí)網(wǎng)絡(luò)圖��,請(qǐng)你填寫(xiě)圖中空白
2.用分子���、原子的觀點(diǎn)解釋�����。
(1)水銀體溫計(jì)測(cè)量體溫 (2) 走近酒店附近就能聞到酒的氣味
(3)過(guò)氧化氫分解產(chǎn)生水和氧氣
(二)����、分子�、原子、離子���、元素和物質(zhì)的關(guān)系
3.根據(jù)所學(xué)知識(shí)填寫(xiě)下列關(guān)系圖:
構(gòu)成
構(gòu)成
同
3����、一種元素
組成
總稱(chēng)
原子
物質(zhì)
得失電子
構(gòu)成
構(gòu)成
不同種元素
組成
元素
4.我們生活的世界是由豐富多彩的物質(zhì)組成的,而物質(zhì)又是由微小的粒子構(gòu)成的��。
⑴ 對(duì)于二氧化碳(CO2)我們可以這樣說(shuō):
① 氧化碳是由 組成的����;②二氧化碳是由 構(gòu)成的;③二氧化碳分子是由 構(gòu)成的���;④一個(gè)二氧化碳分子是由 構(gòu)成的���。
⑵ 于汞而言,汞是由 組成的��;汞是由 構(gòu)成的�����。
⑶對(duì)于氯化鈉而言�,氯化鈉是由 組成的;氯化鈉是由 構(gòu)成的�����。
5.用化學(xué)符號(hào)表示或?qū)懗龌瘜W(xué)
4�����、用語(yǔ)的含義
硫離子 2個(gè)氮分子 鋅元素 4個(gè)亞鐵離子
2H2CO3 ���、 (寫(xiě)出兩個(gè)“2”的含義)���。
6.甲、乙是兩種粒子的結(jié)構(gòu)示意圖�,下列說(shuō)法正確的是 ( )
A.甲是陽(yáng)離子
B.乙是陰離子
C.甲、乙屬于不同種元素
D.甲���、乙都屬于金屬元素
三���、自主探究
7. 質(zhì)子數(shù)相同的兩種不同粒子可能是①同一元素的原子或離子②兩個(gè)不同的分子③一種原子和一種
5、分子④兩種不同的離子⑤一種離子和一種分子 ( )
A���、①③ B�����、①②③④ C���、①③④⑤ D、①②③④⑤
8.已知NO2是紅棕色氣體,N2O4是一種無(wú)色氣體���。NO2在密閉容器內(nèi)受壓時(shí)能轉(zhuǎn)化為N2O4氣體����。某同學(xué)設(shè)計(jì)了如圖所示的兩個(gè)實(shí)驗(yàn)探究有關(guān)的變化��。實(shí)驗(yàn)時(shí)甲抽去中間的玻璃片����,乙推壓密閉注射器里的活塞,然后再松開(kāi)��。
甲
6����、 乙
(1)甲實(shí)驗(yàn)產(chǎn)生的實(shí)驗(yàn)現(xiàn)象是 ,該實(shí)驗(yàn)說(shuō)明的問(wèn)題是 ����。
(2)乙實(shí)驗(yàn)觀察到的實(shí)驗(yàn)現(xiàn)象是 ,該變化屬于 變化����。
(3)上述兩個(gè)變化的本質(zhì)區(qū)別是什么? ���。
9.某物質(zhì)在隔絕空氣加熱后�����,生成氧氣和氯化鉀���,由此可證明該物質(zhì)中含有哪些元素?它們是金屬元素�����,還是非金屬元素�?
【中考鏈接】
10.(2020?四川)雖說(shuō)“
7、清明時(shí)節(jié)雨紛紛”�����,可也不乏“她在叢中笑”的風(fēng)景���。此時(shí)的“她”聞到了花香襲人���,其原因是 ( )
A.物理變化中分子大小是不變的 B.原子是化學(xué)變化中的最小粒子
C.原子不可分而分子可分 D.分子在不停地做無(wú)規(guī)則的運(yùn)動(dòng)
11.(2020?四川) 下列敘述正確的是 ( )
A. 水結(jié)冰后分子停止運(yùn)動(dòng) B. 氯化鈉晶體由氯化鈉分子構(gòu)成
C. 氫
8����、原子和氧原子保持水的化學(xué)性質(zhì) D. 氧化汞分子在化學(xué)變化中能夠再分
12.(2020.湘潭市)右圖是甲�����、乙兩種粒子的結(jié)構(gòu)示意圖���,下列有說(shuō)法正確的是 ( )
甲 乙
A.甲粒子是陽(yáng)離子
B.乙粒子是原子
C.兩種粒子屬于同種元素
D.甲粒子的化學(xué)性質(zhì)比乙粒子穩(wěn)定
【反思與小結(jié)】
(1)物質(zhì)由 組成�,同時(shí)又是由 �、 、 構(gòu)成��。
(2)原子的質(zhì)量主要集中在 �;決定元素化學(xué)性質(zhì)的是 ;決定元素種類(lèi)的是 ����。
(3)在元素符號(hào)前加上數(shù)字
9、后只能有微觀意義�,沒(méi)有宏觀意義。
四�����、自我測(cè)評(píng)
1.下列有關(guān)原子與離子的說(shuō)法不正確的是 ( )
A.質(zhì)子數(shù)相同的原子與離子的化學(xué)性質(zhì)是不同的
B.離子可以通過(guò)得或失電子而變成原子
C.原子變成離子時(shí)���,電子層數(shù)一定發(fā)生改變
D.帶電的原子被稱(chēng)為離子
2.用其質(zhì)量的1/12作為相對(duì)原子質(zhì)量的標(biāo)準(zhǔn)的碳原子相對(duì)原子的質(zhì)量是 ( ?��。?
A.12g B.12 C.1/12g D.1/12
3.分析各組微粒結(jié)構(gòu)示意圖���,與表示的意義一致的是 ( )
A.都屬于陽(yáng)離子 B.都屬于陰離子
 重慶市璧山縣青杠初級(jí)中學(xué)校九年級(jí)化學(xué)上冊(cè) 第三單元 課題1 分子和原子復(fù)習(xí)學(xué)案(無(wú)答案)(新版)新人教版
重慶市璧山縣青杠初級(jí)中學(xué)校九年級(jí)化學(xué)上冊(cè) 第三單元 課題1 分子和原子復(fù)習(xí)學(xué)案(無(wú)答案)(新版)新人教版